NAT CATAL丨酶-DNA动态网络实现可控生物催化的级联反应
作者:张铭芷
物理学致力于揭示宇宙定律,生物学旨在掌握生命的秘密。尽管前者可以解释非生命和生命事物的一般规则,却忽视了它们的本质区别。而后者在无法解释其原始起源的情况下仍然遵循一定的规则控制着复杂的生物。人类从物理学到生物学间知识的鸿沟应如何跨越?如何捋清从无生命到有生命物质的逻辑线程?
我们知道,细胞的许多转化过程如同化作用、异化作用都是由酶的相互作用、代谢甚至到DNA层面的复杂调节网络完成的。11月12日在Nature Ctalysis发布的研究文章中,Itamar Willner课题组设计了一种基于酶-DNA动态网络响应外部刺激,进而稳定到合适状态的体外模拟体系。
诺奖得主Lehn于2007年提出的概念中,从非生命到生命的分子具有自我组织系统以应对紧急状况的特性。这种系统由可逆反应连接的化学物种网络组成,根据它们是否共享一个组成部分,将它们设定成竞争或相互转换的关系。这种组分动态网络(CDN)可以以初始逻辑线程和自组织系统的形式实现感应环境信号并完成响应。这种系统可以表示为最简单的四组分系统: A、B、A’和B’,它们组成四个不同的组分AA’、AB’、BA’和BB’。在热力学平衡下,系统由所有组分的固定含量表示。由于这些组分相互连接,通过物理刺激或化学效应器对网络的一个组分进行扰动,将导致系统中各个组分含量的再分配,直到达到新的平衡状态。例如,AA’组分的增加(或减少)将推动直接连接组分(即拮抗剂AB’和BA’)的向下(或向上)调节。同时,也将改变与目标没有直接联系的相关组分BB‘,而其将遵循与AA‘相同的调节,也就是说,它将上调(或下调)。这种以牺牲为代价的生存法则遵循了达尔文主义原则,体现了进化能力。
在前人的研究中,对这一概念的实施仅限于结构转型,除了读出信号之外并不能实现真正的外部环境运作,即赋予适当的功能。而Itamar Willner课题组的工作克服了这一限制。利用与葡萄糖氧化酶(GOx)和辣根过氧化物酶(HRP)功能化的核酸成分,研究人员生成一个基于DNA的动态网络,其可逆触发的重新配置可产生GOx/HRP催化级联的可切换上下调节。
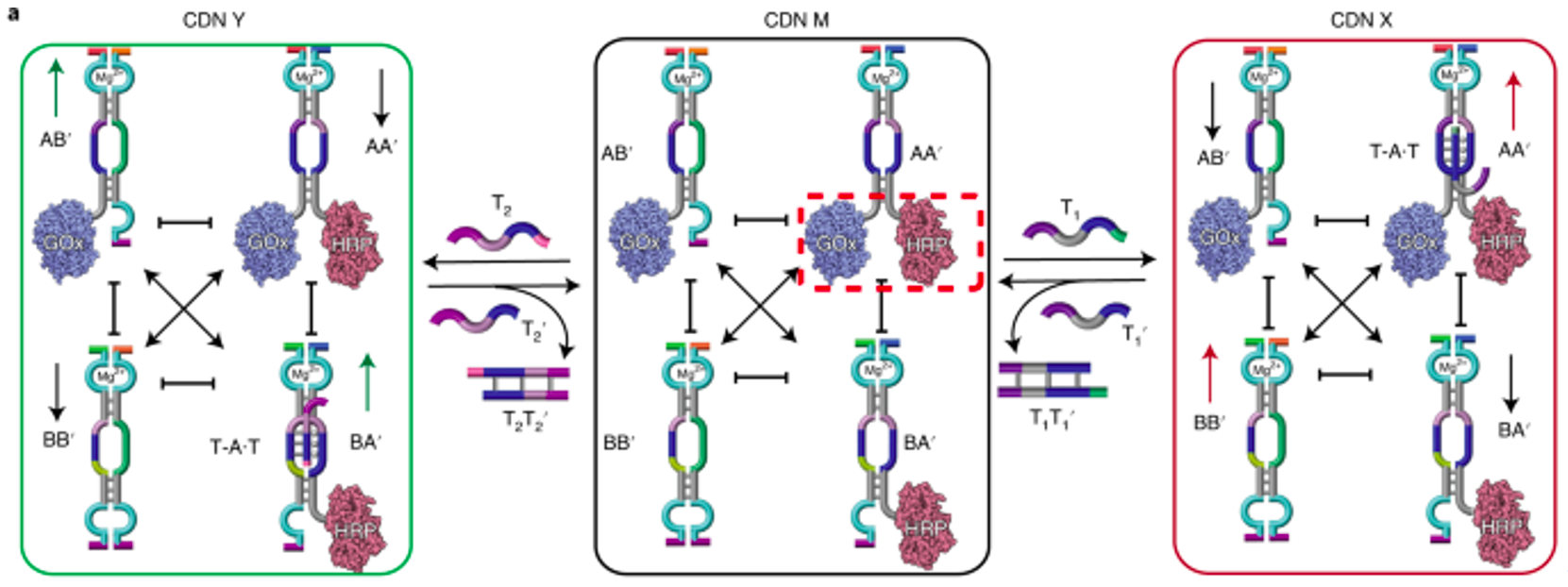
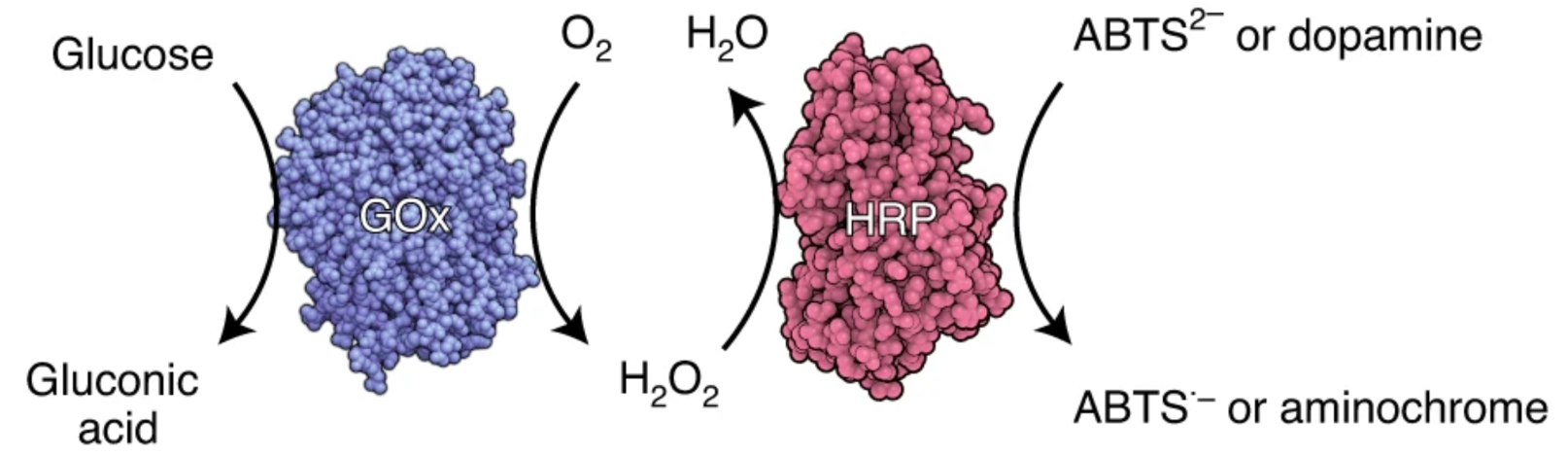
与Lehn最初开发的四组分模型类似,此处描述的系统由四个核酸成分组成:其中两个与级联(GOx-A或HRP-A’)的单个酶结合,而另外两个则为无酶(B和B’)。在平衡时,反应混合物包含四种:GOx/HRP-AA’、GOx-AB’、BA’-HRP和BB’。成分AA’中两种酶的空间接近允许层联操作,在葡萄糖和氧气的存在的情况下使得将ABTS2–被氧化成Abts•–或将多巴胺氧化成胺色素。
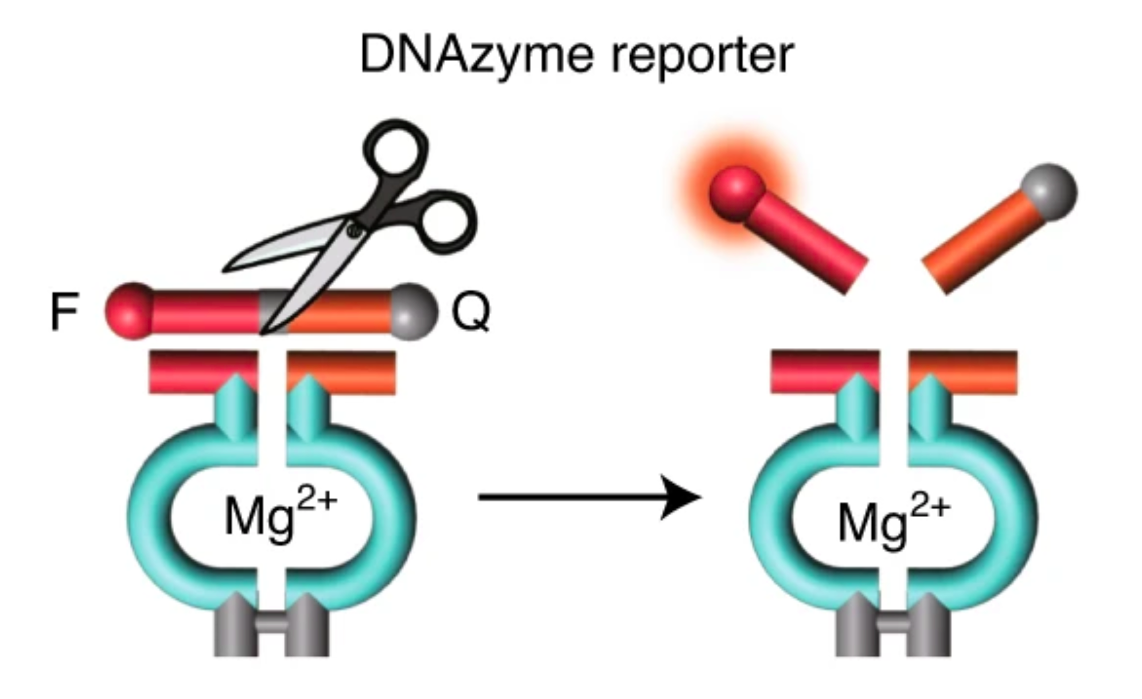
此外,DNA网络还具有两个重要特征。首先,每个组分包括一个结合的Mg2-依赖的DNAzyme单元充当报告系统,以量化系统中相应组分的内容。其次,每个组成包含一个不同的开放可循环区域,在辅助触发器T1(或T2)存在的情况下,组分AA’(或BA’)被稳定成三链结构。在这个系统中,Mg2+依赖域能够将生物催化级联的效率与每个组分的含量关联,而三链稳定区域是使切换行为成为可能的基本原因。
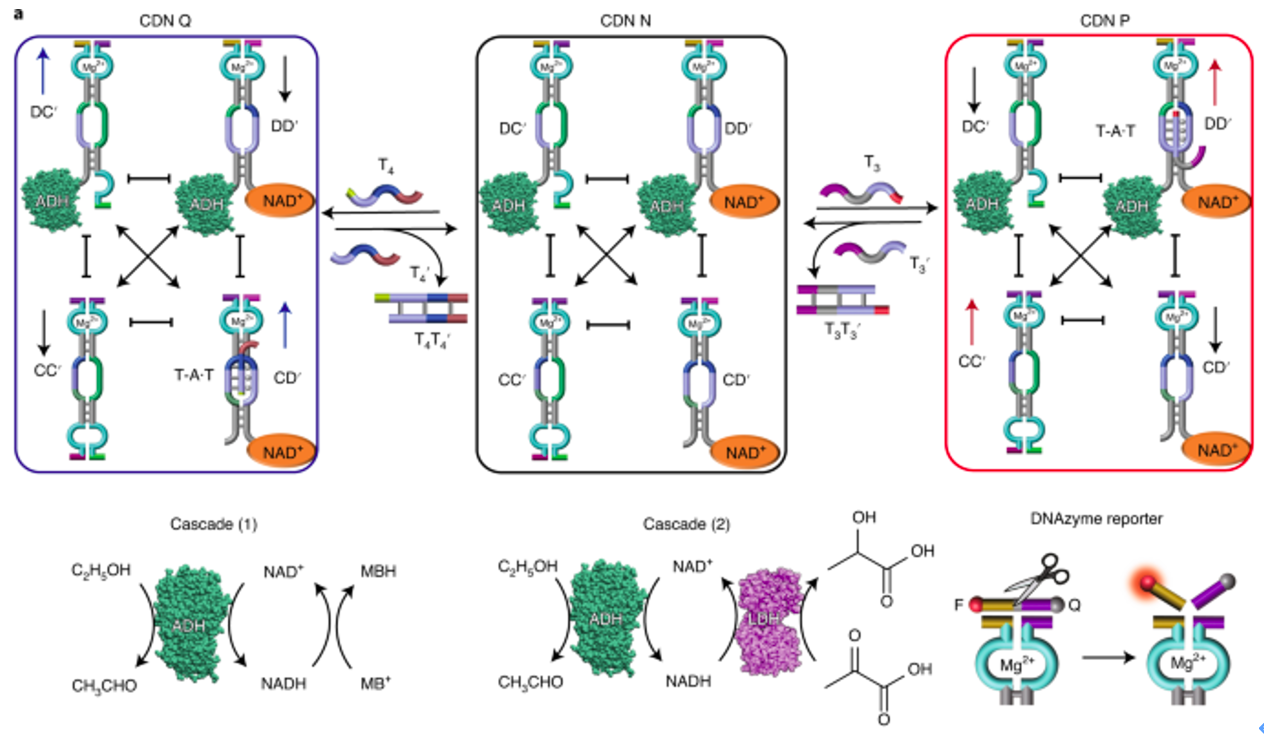
接下来,研究人员用类似的方法设计了辅酶因子的级联调控网络。同样地,各个组分依赖Mg2+结构域以及DNAzyme构成组分含量的报告系统,通过辅助触发器T3或T4稳定其中某一组分从而刺激系统使得系统平衡移动,最后达到各个组分含量的重新分配。
以上两类级联网络均是基于双酶或酶和辅酶因子组合相互作用的二维系统。为了建立一个三维互作网络,使得级联网络系统更为复杂且更贴近实际情况,研究人员设计了由两个子级联系统相互作用组成的大级联系统,即将上述两个系统合并对其施行正交操作。
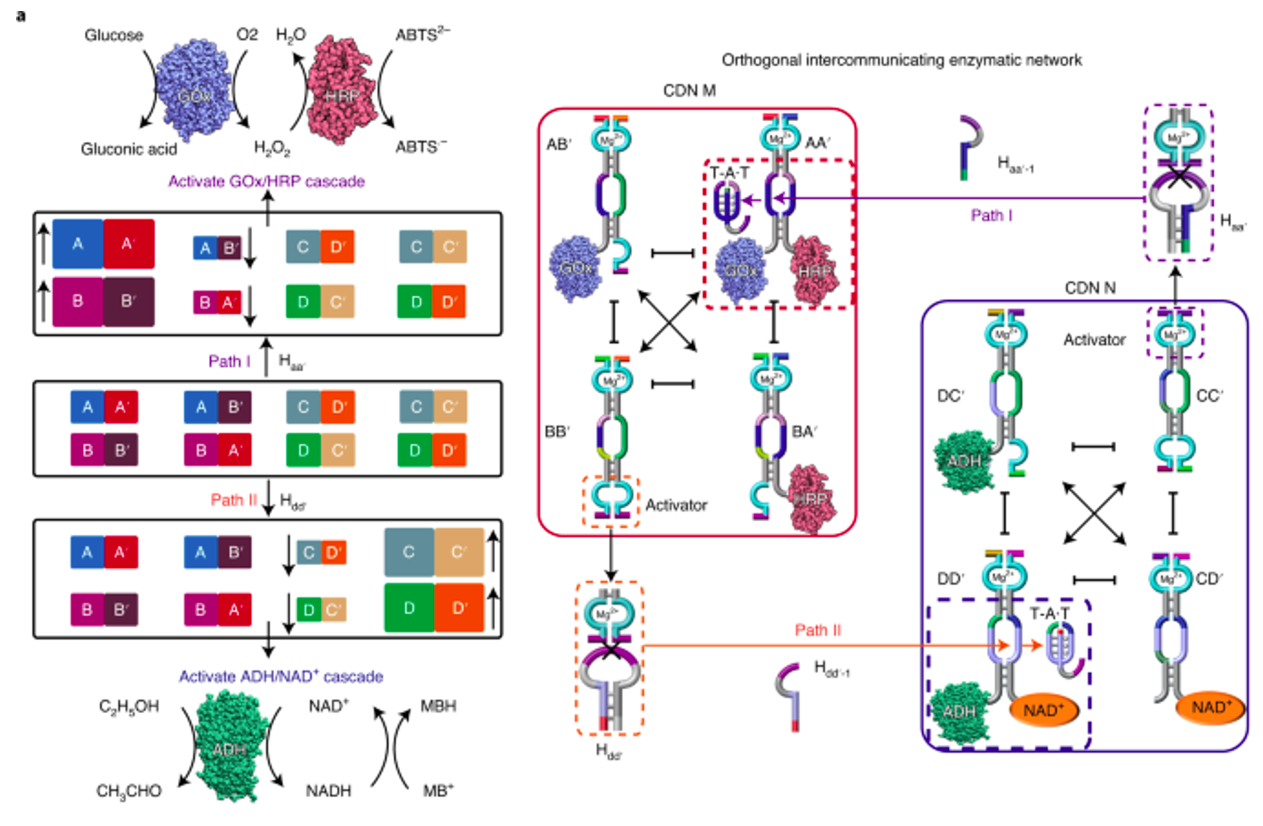
设计中引入了发夹结构H作为辅助触发器的前体,形成辅助触发器T的原理与前文所述报告器的工作原理类似。通过发夹结构H可以介导两正交子生物催化级联网络的相互影响。接下来,研究人员通过计数器网络生成的触发器链成功控制一个网络的级联催化活动,设计了CDN N和CDN M的反馈驱动、耦合、时间依赖的通信。通过发夹H的时间依赖的浓度变化控制(即动力学控制)可进行子网络间的耦合、反馈和通信控制。
综上所述,该研究引入了由酶核酸或辅助因子核酸组成的混合系统作为功能组件,构建能够证明对生物催化级联的控制的组分动态网络。所集成的生物催化器之间的空间接近为生物催化级联变换增添了新的维度。生物催化级联通过辅助触发器控制CDN中成分的组成,从而证明了生物催化级联网络的上调节或降低的触发条件。此外,研究报告中的一项重大进展涉及两个网络之间的相互通信,以及通过邻近网络在一个网络中对另一正交生物催化级联的耦合控制,为通过网络通信控制生物催化级联的反馈机制为放大级联催化网络的运行和决定级联生物催化转化的动力学提供了一个概念。这些成就为系统化学领域引入了基本概念,因为它们为自然过程提供了复杂的动态模型系统,系统可能提示潜在的癌症催化治疗相关的应用。
Wang, C., Yue, L. & Willner, I. Controlling biocatalytic cascades with enzyme–DNA dynamic networks. Nat Catal 3, 941–950 (2020). https://doi.org/10.1038/s41929-020-00524-7

